Una, ang istraktura at mga katangian ng SiC crystal.
Ang SiC ay isang binary compound na nabuo ng Si element at C element sa 1:1 ratio, iyon ay, 50% silicon (Si) at 50% carbon (C), at ang basic structural unit nito ay SI-C tetrahedron.
Schematic diagram ng silicon carbide tetrahedron structure
Halimbawa, ang mga atomo ng Si ay malaki ang diyametro, katumbas ng isang mansanas, at ang mga atomo ng C ay maliit ang diyametro, katumbas ng isang kahel, at ang isang pantay na bilang ng mga dalandan at mansanas ay pinagsama-sama upang bumuo ng isang kristal na SiC.
Ang SiC ay isang binary compound, kung saan ang Si-Si bond atom spacing ay 3.89 A, paano maintindihan ang spacing na ito? Sa kasalukuyan, ang pinakamahusay na makina ng lithography sa merkado ay may katumpakan ng litograpiya na 3nm, na isang distansya na 30A, at ang katumpakan ng litograpiya ay 8 beses kaysa sa distansya ng atomic.
Ang enerhiya ng bono ng Si-Si ay 310 kJ/mol, kaya mauunawaan mo na ang enerhiya ng bono ay ang puwersa na humihila sa dalawang atom na ito, at kung mas malaki ang enerhiya ng bono, mas malaki ang puwersa na kailangan mong paghiwalayin.
Halimbawa, ang mga atomo ng Si ay malaki ang diyametro, katumbas ng isang mansanas, at ang mga atomo ng C ay maliit ang diyametro, katumbas ng isang kahel, at ang isang pantay na bilang ng mga dalandan at mansanas ay pinagsama-sama upang bumuo ng isang kristal na SiC.
Ang SiC ay isang binary compound, kung saan ang Si-Si bond atom spacing ay 3.89 A, paano maintindihan ang spacing na ito? Sa kasalukuyan, ang pinakamahusay na makina ng lithography sa merkado ay may katumpakan ng litograpiya na 3nm, na isang distansya na 30A, at ang katumpakan ng litograpiya ay 8 beses kaysa sa distansya ng atomic.
Ang enerhiya ng bono ng Si-Si ay 310 kJ/mol, kaya mauunawaan mo na ang enerhiya ng bono ay ang puwersa na humihila sa dalawang atom na ito, at kung mas malaki ang enerhiya ng bono, mas malaki ang puwersa na kailangan mong paghiwalayin.
Schematic diagram ng silicon carbide tetrahedron structure
Halimbawa, ang mga atomo ng Si ay malaki ang diyametro, katumbas ng isang mansanas, at ang mga atomo ng C ay maliit ang diyametro, katumbas ng isang kahel, at ang isang pantay na bilang ng mga dalandan at mansanas ay pinagsama-sama upang bumuo ng isang kristal na SiC.
Ang SiC ay isang binary compound, kung saan ang Si-Si bond atom spacing ay 3.89 A, paano maintindihan ang spacing na ito? Sa kasalukuyan, ang pinakamahusay na makina ng lithography sa merkado ay may katumpakan ng litograpiya na 3nm, na isang distansya na 30A, at ang katumpakan ng litograpiya ay 8 beses kaysa sa distansya ng atomic.
Ang enerhiya ng bono ng Si-Si ay 310 kJ/mol, kaya mauunawaan mo na ang enerhiya ng bono ay ang puwersa na humihila sa dalawang atom na ito, at kung mas malaki ang enerhiya ng bono, mas malaki ang puwersa na kailangan mong paghiwalayin.
Halimbawa, ang mga atomo ng Si ay malaki ang diyametro, katumbas ng isang mansanas, at ang mga atomo ng C ay maliit ang diyametro, katumbas ng isang kahel, at ang isang pantay na bilang ng mga dalandan at mansanas ay pinagsama-sama upang bumuo ng isang kristal na SiC.
Ang SiC ay isang binary compound, kung saan ang Si-Si bond atom spacing ay 3.89 A, paano maintindihan ang spacing na ito? Sa kasalukuyan, ang pinakamahusay na makina ng lithography sa merkado ay may katumpakan ng litograpiya na 3nm, na isang distansya na 30A, at ang katumpakan ng litograpiya ay 8 beses kaysa sa distansya ng atomic.
Ang enerhiya ng bono ng Si-Si ay 310 kJ/mol, kaya mauunawaan mo na ang enerhiya ng bono ay ang puwersa na humihila sa dalawang atom na ito, at kung mas malaki ang enerhiya ng bono, mas malaki ang puwersa na kailangan mong paghiwalayin.
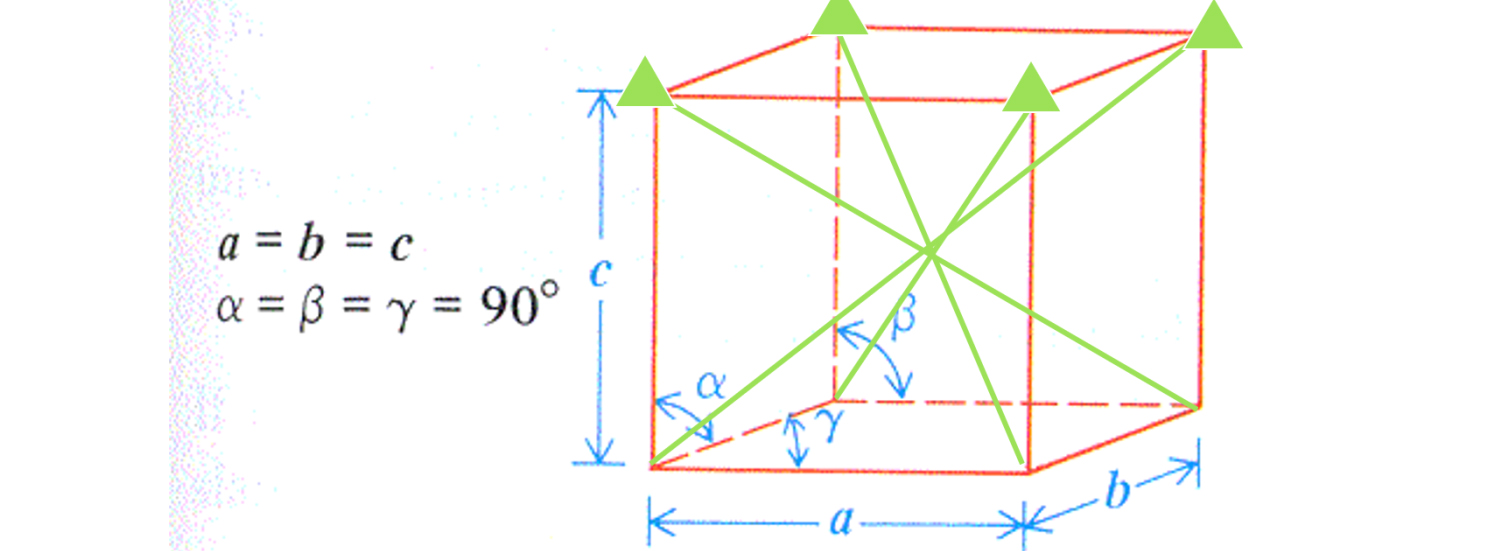
Alam natin na ang bawat sangkap ay binubuo ng mga atomo, at ang istruktura ng isang kristal ay isang regular na pag-aayos ng mga atomo, na tinatawag na isang long-range order, tulad ng mga sumusunod. Ang pinakamaliit na yunit ng kristal ay tinatawag na isang cell, kung ang cell ay isang kubiko na istraktura, ito ay tinatawag na isang close-packed na kubiko, at ang cell ay isang heksagonal na istraktura, ito ay tinatawag na isang close-packed na heksagonal.
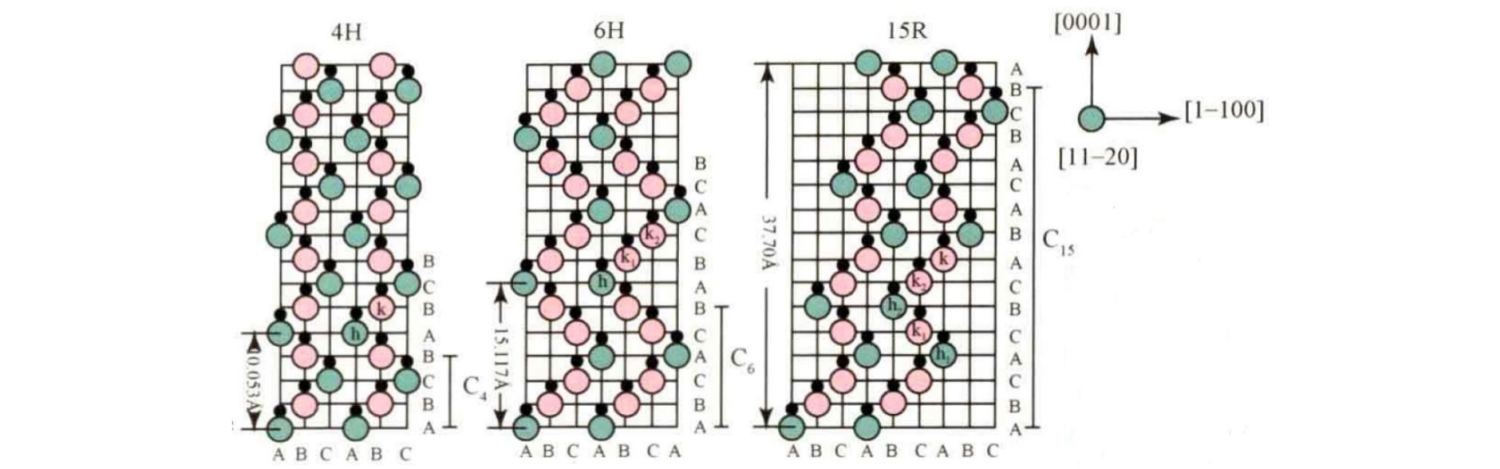
Kasama sa mga karaniwang uri ng kristal ng SiC ang 3C-SiC, 4H-SiC, 6H-SiC, 15R-SiC, atbp. Ang kanilang pagkakasunod-sunod ng stacking sa direksyon ng c axis ay ipinapakita sa figure.
Kabilang sa mga ito, ang pangunahing pagkakasunud-sunod ng stacking ng 4H-SiC ay ABCB... ; Ang pangunahing stacking sequence ng 6H-SiC ay ABCACB... ; Ang pangunahing stacking sequence ng 15R-SiC ay ABCACBCABACABCB... .
Ito ay makikita bilang isang ladrilyo para sa pagtatayo ng isang bahay, ang ilan sa mga ladrilyo sa bahay ay may tatlong paraan ng paglalagay nito, ang ilan ay may apat na paraan ng paglalagay nito, ang ilan ay may anim na paraan.
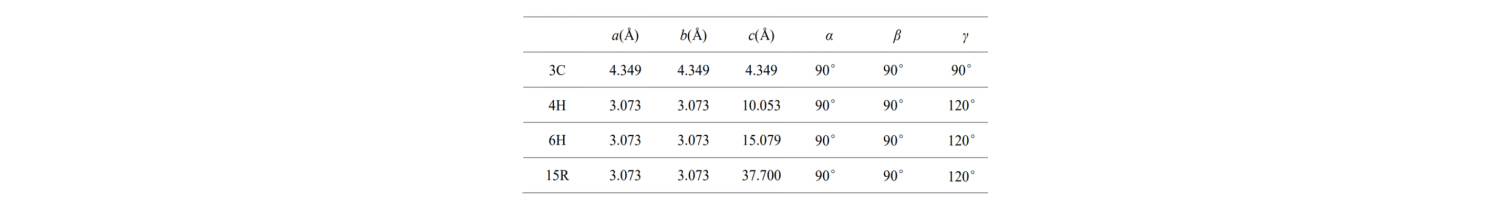
Ang mga pangunahing parameter ng cell ng mga karaniwang uri ng kristal na SiC ay ipinapakita sa talahanayan:
Ano ang ibig sabihin ng a, b, c at anggulo? Ang istraktura ng pinakamaliit na yunit ng cell sa isang SiC semiconductor ay inilarawan bilang mga sumusunod:
Sa kaso ng parehong cell, ang istraktura ng kristal ay magkakaiba din, ito ay tulad ng pagbili natin ng lottery, ang nanalong numero ay 1, 2, 3, bumili ka ng 1, 2, 3 tatlong numero, ngunit kung ang numero ay pinagsunod-sunod. iba, iba ang nanalong halaga, kaya ang numero at pagkakasunud-sunod ng parehong kristal, ay matatawag na parehong kristal.
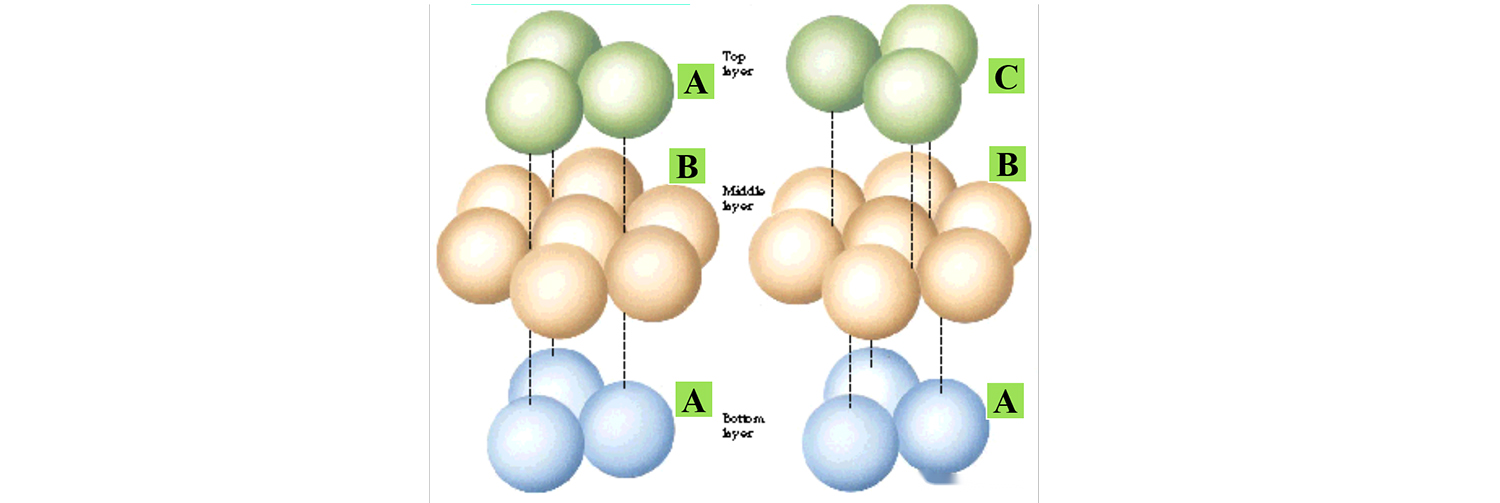
Ang sumusunod na figure ay nagpapakita ng dalawang tipikal na stacking mode, tanging ang pagkakaiba sa stacking mode ng itaas na atoms, ang kristal na istraktura ay naiiba.
Ang istraktura ng kristal na nabuo ng SiC ay malakas na nauugnay sa temperatura. Sa ilalim ng pagkilos ng mataas na temperatura ng 1900~2000 ℃, dahan-dahang magbabago ang 3C-SiC sa hexagonal SiC polyform tulad ng 6H-SiC dahil sa hindi magandang structural stability nito. Ito ay tiyak na dahil sa malakas na ugnayan sa pagitan ng posibilidad ng pagbuo ng SiC polymorphs at temperatura, at ang kawalang-tatag ng 3C-SiC mismo, ang rate ng paglago ng 3C-SiC ay mahirap mapabuti, at ang paghahanda ay mahirap. Ang hexagonal system ng 4H-SiC at 6H-SiC ay ang pinakakaraniwan at mas madaling ihanda, at malawak na pinag-aaralan dahil sa kanilang sariling mga katangian.
Ang haba ng bono ng SI-C bond sa SiC crystal ay 1.89A lamang, ngunit ang nagbubuklod na enerhiya ay kasing taas ng 4.53eV. Samakatuwid, ang agwat ng antas ng enerhiya sa pagitan ng estado ng pagbubuklod at ng estado ng anti-bonding ay napakalaki, at maaaring mabuo ang isang malawak na agwat ng banda, na ilang beses kaysa sa Si at GaAs. Ang mas mataas na lapad ng band gap ay nangangahulugan na ang mataas na temperatura na istraktura ng kristal ay matatag. Maaaring mapagtanto ng nauugnay na power electronics ang mga katangian ng matatag na operasyon sa mataas na temperatura at pinasimple na istraktura ng pagwawaldas ng init.
Ang mahigpit na pagbubuklod ng Si-C bond ay ginagawang ang sala-sala ay may mataas na dalas ng panginginig ng boses, iyon ay, isang mataas na enerhiya na phonon, na nangangahulugan na ang SiC crystal ay may mataas na saturated electron mobility at thermal conductivity, at ang mga nauugnay na power electronic device ay may isang mas mataas na bilis ng paglipat at pagiging maaasahan, na binabawasan ang panganib ng pagkabigo sa sobrang temperatura ng device. Bilang karagdagan, ang mas mataas na lakas ng field ng breakdown ng SiC ay nagbibigay-daan dito upang makamit ang mas mataas na konsentrasyon ng doping at magkaroon ng mas mababang on-resistance.
Pangalawa, ang kasaysayan ng pag-unlad ng SiC crystal
Noong 1905, natuklasan ni Dr. Henri Moissan ang isang natural na SiC na kristal sa bunganga, na nakita niyang kahawig ng isang brilyante at pinangalanan itong Mosan na brilyante.
Sa katunayan, noon pang 1885, nakuha ni Acheson ang SiC sa pamamagitan ng paghahalo ng coke sa silica at pag-init nito sa isang electric furnace. Noong panahong iyon, napagkakamalan itong pinaghalong diamante ng mga tao at tinawag itong emery.
Noong 1892, pinahusay ni Acheson ang proseso ng synthesis, pinaghalo niya ang quartz sand, coke, isang maliit na halaga ng wood chips at NaCl, at pinainit ito sa isang electric arc furnace sa 2700 ℃, at matagumpay na nakakuha ng mga scaly na SiC crystal. Ang pamamaraang ito ng pag-synthesize ng mga kristal ng SiC ay kilala bilang pamamaraan ng Acheson at ito pa rin ang pangunahing paraan ng paggawa ng mga abrasive ng SiC sa industriya. Dahil sa mababang kadalisayan ng mga sintetikong hilaw na materyales at magaspang na proseso ng synthesis, ang pamamaraan ng Acheson ay gumagawa ng higit pang mga impurities ng SiC, mahinang integridad ng kristal at maliit na diameter ng kristal, na mahirap matugunan ang mga kinakailangan ng industriya ng semiconductor para sa malalaking sukat, mataas na kadalisayan at mataas. -mga kristal na kalidad, at hindi maaaring gamitin sa paggawa ng mga elektronikong kagamitan.
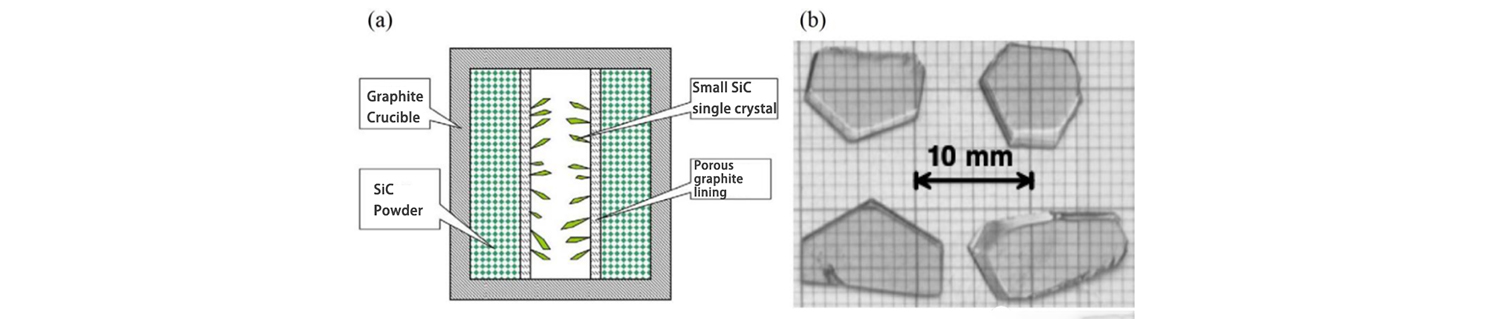
Iminungkahi ni Lely ng Philips Laboratory ang isang bagong paraan para sa pagpapalaki ng mga solong kristal ng SiC noong 1955. Sa pamamaraang ito, ang graphite crucible ay ginagamit bilang sisidlan ng paglaki, ang SiC powder crystal ay ginagamit bilang hilaw na materyal para sa paglaki ng SiC crystal, at ang porous na graphite ay ginagamit upang ihiwalay isang guwang na lugar mula sa gitna ng lumalagong hilaw na materyal. Kapag lumalaki, ang graphite crucible ay pinainit sa 2500 ℃ sa ilalim ng kapaligiran ng Ar o H2, at ang peripheral na SiC powder ay na-sublimed at nabubulok sa Si at C vapor phase substance, at ang SiC crystal ay lumaki sa gitnang guwang na rehiyon pagkatapos ng gas Ang daloy ay ipinapadala sa pamamagitan ng porous graphite.
Pangatlo, teknolohiya ng paglago ng SiC crystal
Ang solong paglaki ng kristal ng SiC ay mahirap dahil sa sarili nitong mga katangian. Ito ay higit sa lahat dahil sa ang katunayan na walang likidong bahagi na may stoichiometric ratio ng Si: C = 1: 1 sa atmospheric pressure, at hindi ito maaaring palaguin ng mga mas mature na paraan ng paglago na ginagamit ng kasalukuyang pangunahing proseso ng paglago ng semiconductor industriya - pamamaraan ng cZ, paraan ng pagbagsak ng crucible at iba pang mga pamamaraan. Ayon sa teoretikal na pagkalkula, kapag ang presyon ay mas malaki kaysa sa 10E5atm at ang temperatura ay mas mataas kaysa sa 3200 ℃, ang stoichiometric ratio ng Si: C = 1:1 na solusyon ay maaaring makuha. Upang malampasan ang problemang ito, ang mga siyentipiko ay gumawa ng walang humpay na pagsisikap na magmungkahi ng iba't ibang paraan upang makakuha ng mataas na kalidad ng kristal, malalaking sukat at murang mga kristal na SiC. Sa kasalukuyan, ang mga pangunahing pamamaraan ay PVT method, liquid phase method at high temperature vapor chemical deposition method.
Oras ng post: Ene-24-2024